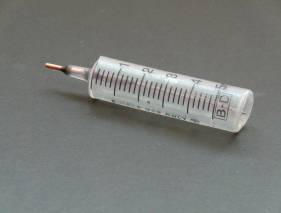
傳統中學化學實驗非電子式定量儀器多是簡單的滴定管、移液管、量筒、針管、秒表等。目前市面很多套件微型化學實驗儀器以一盒多件形式出售。大部份套件以塑料滴管、微型電解裝置、井穴反應板塊等為主要配件,可以作定量性測試的不多。因此有需要創新設計針對某課程實驗之微型定量儀器。
4.1 8井穴反應條 (8-well reaction strip) 及建議實驗 (11) 和 (12)
平底透明 8 井穴反應條 (圖 63) 微型化學實驗並不是新事物,早在數十年前北美國家中學已經採用了,但並不是用作主流實驗儀器。它有一個特點是把載有液體之井穴條倒轉後,在水面張力作用下,液體不會掉下來 (圖 64)。其他較大容量之井穴條不具這特性。
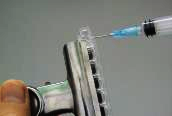
平底透明塑料8井穴反應條及其相關板塊 (圖 65) 是醫學化驗所必備之工具。可購買之平底透明塑料8井穴反應條很容易被折斷 (圖 66),不宜直接作學生實驗用。用一透明亞加力膠條施加小量化膠水 (即哥羅芳或三氯甲烷) (圖 67) 可令反應條變得堅固,不容易折斷。
(圖 64) 液體不會掉下來 | ||
(圖 66) 條塊容易折斷 | (圖 67) 用針筒施小量化膠水於井穴條和亞加力膠條之間 |
8井穴反應條在微型化學實驗有一特別用途。
一般化學反應速率實驗要在反應物溶液在不同濃度下進行個別實驗記錄反應時間,起碼實驗4 次 才可以作定量調研,要化一定時間。但如果利用 8 井穴反應條內之液體不下掉特性和一種叫 「下搖」 技巧 (“shake-down” technique),便可以在 同一時間 內做數次不同濃度之反應速率實驗,節省不少時間。
方法是置 9 小滴反應物於每一井穴之 A 條,也放置同容量之另一反應物於每一井穴之 B 條。輕輕倒置 A 條,小心覆蓋 A 條於 B 條上,並須使兩者之八個井穴都互相對準。雙手握住兩端,然後猛力把兩井穴條向下一搖,使 B 條的溶液落入 A 條內。最少兩次把 A 條和 B 條上下搖動確保溶液徹底混合 (「下搖」 技巧) 產生反應 (圖 68) 。

(圖 68) 「下搖」 技巧
DSE化學科課程課題九 “反應速率” 和課題十三 “工業化學” 都有涉及影響化學反應速率各種量化因素 ,如濃度 、温度等 。8穴反應條微型儀器對測定反應級數有獨特優點 ,可以極速測定速率與各反應物溶液濃度之量化關係 ,從而建立速率方程 。操作既有微量之特性,也有只用兩分鐘時間便可以完成整個實驗之快速測定優勢。
「碘時鐘反應」(詳述參閱實驗11) 之主體反應是H2O2 (aq) 和I– (aq) 離子氧化還原反應,化學方程為:
H2O2(aq) + 2I-(aq) + 2H+(aq) → I2(aq) + 2H2O(l)
反應物濃度改變和反應速率改變有正比例關係,其量化程度不只限於大和小兩種。應有一方程式,以濃度變數數字代入,可 計算 反應速率。反應速率和反應物濃度之量化方程式為:
Rate = k[I-(aq)][H2O2(aq)]
k 為反應常數。對 I–(aq) 離子和 H2O2(aq) 均為 1 級反應,對 H+(aq) 離子為 0 級反應而反應總級數為 2。利用 8 井穴反應條特性和創新之「1 2 4 8」 技巧,可巧妙地極速測定「碘時鐘反應」之各反應物之反應級數。
要注意一點:
因反應物用量微少,實驗结果很大程度取決於用量之準確性。以滴數取代容積實數,各滴容積會不一樣,因此微型實驗誤差會比一般傳統實驗誤差高。補救方法是多做幾次,取其平均值。
實驗 (11) 過氧化氫與碘離子在酸性溶液中的反應總級數(88頁)
「碘時鐘反應」
實驗 (12) 微型定量測定酸化硫代硫酸鈉之反應速率 (95頁) ,「消失交叉」

(圖 69)「消失交叉」實驗
4.2 小型加熱器快速測定 (碘時鐘反應) 活化能 (activation energy) 及建議實驗 (13)
量化反應速率或建立反應速率方程基本上要量化速率與溶液濃度和溫度之關係。主題 4.1 及建議實驗已探究了速率與個別及總反應物濃度反應級數 (kinetic order) 之關係。碘時鐘反應之速率方程式為 速率 = k[I(aq)–][H2O2],k 為速率常數。其實這方程只顯示速率與濃度之量化關係,沒有速率與溫度之量化關係。事實 k 並不是某反應常數,而是某反應速率與溫度的變數。速率常數和溫度之定量關係以阿列紐斯方程 (Arrhenius equation) 量化:k = Ae 其中 ΔHact為活化能 (activation energy),對某反應是一常數,數值越小,反應速率越快。A 和 R 均為通用常數。對數式方程為:
k = Ae ![]()
其中 ΔHact 為活化能 (activation energy),對某反應是一常數,數值越小,反應速率越快。A 和 R 均為通用常數。對數式方程為:
ln(k) = ln(A) –![]()
速率常數 k (k 可視為反應物濃度皆為單位數時之反應速度) ,和反應時間 t 成反比例,即 1/t。因此 ln(k) 和 ln(1/t) 也成比例。以上對數式方程可改寫為:
ln(1/t) = ln(A) –![]()
以ln (1/t) vs (1/T) 作一直線圖解,其斜率為 – ΔHact/R,從而計算 ΔHact。
綜合主題 4.1和 4.2,可以得出碘時鐘反應之完整速率方程式為:
Rate = (Ae![]() )([I-(aq)][H2O2(aq)])
)([I-(aq)][H2O2(aq)])
儀器製作
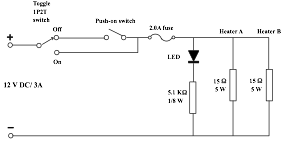
使用明火或水浴是中學實驗室常用的加熱水溶液方法 。若要求溶液準確地達到某一溫度,上述方法都很難辦到。理想方法是緩慢而反覆地加熱,例如電力恆溫水浴器 (automatic thermostat) 。使用低功率電阻低電壓,反覆地,慢慢地直接加熱溶液也可以達到目的 。電阻作為發熱器用以線阻最好 。以下電路以水泥電阻內之5W線阻發熱 (圖 70) 。
(圖 70) 小型加熱器線路圖
儀器组成: 一對小型電力加熱器 (探測器) (圖 72) 和一個控制面板 (圖 71) 。需要12V DC低壓電源 (12V AC也可以,但 LED 指示燈不會亮)。
 |  |  |
(圖 71) | (圖 72) | (圖 73) |
1. 小型電力加熱器
首先用硬物砸碎兩支阻值一樣之15 Ω 5W水泥電阻,取出內藏之線阻 (圖 74)。如 (圖 75) 和 (圖 76) 所示,用多層收縮膠圓通箍死。注意不要讓接線短路和 100%防水。探測器就是這樣的一對小型電力加熱器 (圖 77)
另一點更要注要的是只有在加熱器完全浸入水溶液情況下才可以通電加熱。
(圖74) | (圖75) | (圖76) | (圖77) |
2. 控制面板
控制面板主要為一預先鑽了數孔之木板和兩條鋁角 (圖 78和 79) 組成。需要之零件:
名稱 | 數量 |
| 5 mm黃色 LED 連座 | 1 |
| 黑色香蕉插座 | 4 |
| 二刀二擲切換開關 | 1 |
| 按鍵開關 (按下開/放手關) | 1 |
| 2A 保險絲連座 | 1 |
| 5 kΩ 1/8W 碳阻 | 1 |
首先把各類零件依不同位置用鉗子固定 (圖 80) ,用螺絲釘把鋁角上在木板
兩邊。按線路圖 (圖 70) 用電線把各接線點焊好 (圖 73) 。
(圖78) | (圖79) | (圖80) |
3. 儀器操作
注要:只有在加熱器完全浸入水溶液情況下才可以通電加熱
先把控制板面接上低壓電源,再把加熱探測器,一對香蕉插 (輸入A) 跟另一對香蕉插 (輸入B) 插好。A 加熱探測器放入大試管內有反應物 A 溶液。B 加熱探測器放入另一大試管內有容量一樣之反應物 B 溶液。置溫度計於其中一大試管。放置兩大試管於一燒杯,作隔熱用 (圖 81)。整個裝置如 (圖 82) 所示。通電第一步是啟動二刀二擲切換開關,待溶液 A 溫度上升至稍低於目標溫度後,關上二刀二擲切換開關,跟着重覆按下/放手按鍵開關直至剛好到達目標溫度。請參考實驗 (13) 實驗步驟。
| (圖81) | (圖82) |
實驗 (13) 過氧化碘時鐘反應活化能 (100頁)
4.3 微型相對分子質量套件 (RMM kit) 及建議實驗 (14)
儀器說明
課題九“反應速率” 有题及摩爾體積為 24 dm3之計算。微型相對分子質量套件(圖83) 為一創新快速測定常温常壓下丁烷相對分子質量之微型儀器。計算公式用PV = ( ) RT。若已知丁烷之相對分子質量 (M),可以計算常溫常壓摩爾體積常數 (24 dm3)。
若稱量出某氣體體積(V) 之重量 (m),則可計算出氣體之相對分子量 (M) 。RMM套件之實驗誤差率少於5%,實驗值非常接近文獻参考數據。若秤量器用分析度0.001克電子天枰,實驗值會更為準確。
套件可用作學生實驗,也可由顯視儀作實時投影示範。
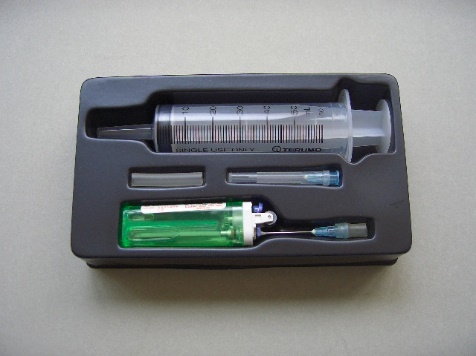
(圖 83) 微型相對分子質量套件
| 套件組件有: |
|
 | 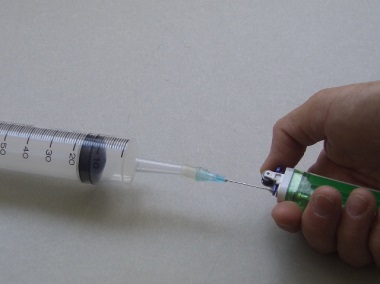 |  |
(圖84) | (圖85) | (圖86) |
儀器操作非常簡單。
| 步驟: | 1. 首先稱量丁烷打火機/針咀組合 (準確度±01克) (圖 84)。 2. 緩緩釋放丁烷至塑膠針筒,直至收集60 cm3 (圖 85)。 3. 再次稱量丁烷打火機/針咀組合 (圖 86)。 4. 假設常温常壓下之摩爾體積為24 dm3,基於所測量之丁烷質量和體積,試計算丁烷之相對分子質量。 |
實驗結果和計算
丁烷打火機/針咀組合之起始質量 = 12.89 g
丁烷打火機/針咀組合之最後質量 = 12.75 g
釋放丁烷之質量 = 0.14 g
釋放丁烷之體積 = 60 ml
丁烷之相對分子質量 = [0.14 x 2400/60 ] = 56 g mol-1
(文獻數據:(C4H10),相對分子質量 = 58 g mol-1)
實驗百分比誤差率 = [(58-56/58) x 100]% = 3.4%
備註
丁烷打火機之噴咀用「超能膠」與注射針咀牢固地粘在一起。丁烷打火機可在各超級市場購買,要選擇那些可放上吸塑膠盆。
實驗 (14) 測定常溫常壓 (r.t.p.)下之氣體常數,R (105頁)
Releasing butane gas
4.4 「電解管」 (electrolysis tube) 及建議實驗 (15)
各地不同化學科課程都包括電解水這一課題。內容基本要求學生知道水可被直流電分解為氫氣和氧氣。釋放之氣體容積比例為 氫(2):氧(1)。電解化學式為:
負極 (-): 4H+(aq) + 4e- → 2H2(g)
陽極(+): 4OH-(aq) – 4e- → O2(g) +2H2O(l)
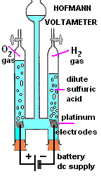
釋放之氧氣可重燃暗紅木條 ,而氫氣則可以引起 “爆鳴” 反應 。一般中學化學實驗室之電解儀器,用於定量顯示的多是傳統之霍夫曼儀 “Hoffmann apparatus”,較為昂貴,因使用鉑電極 (圖 87,88)。學生實驗定性用的一般是使用碳棒電極。優㸃是價廉,缺點是容易斷裂,用作正電極也會被釋放之氧氣氧化腐蝕 。
| (Fig. 87) 霍夫曼儀 “Hoffmann apparatus” | (Fig. 88) 霍夫曼儀示意圖 |
課程 (2) 設計之「「電解管」 」(圖 89) 不用碳電極而用鎳鉻合金線,即發熱線 (nichrome wire)。優點是鎳鉻合金棒條作為電解正極不容易被氧化 (發熱線加熱至熾熱後冷卻回室溫會變為原狀,沒有腐蝕現象)。缺點是電解質溶液只何以用氫氧化鈉溶液而不何以用其他電解質溶液,因為鎳鉻合金線會對其他電解質溶液釋放之氣體有化學反應。中學化學科課程強調水溶液的電解總體,即釋於放氫,氧和兩者之容積比例。其他可能出現之產物皆要借助電化序 (electrochemical series) 之離子釋放次序解釋。採用氫氧化鈉溶液做實驗一則符合設計需要,二則應對DSE化學課程七要求。設備還可作為一簡單氫氧燃料電池。

(圖89)「電解管」
儀器製作
(1) 準備以下物料:(i) 兩枝一次性 5 cm3 針筒 (圖 90),(ii) 透明熱縮膠條,(iii) SWG 16 號銅棒,(iv) 鎳鉻合金線 (圖 91),(v) (A+B) 型金屬填料混合膠
(2) 用小鋸去掉 5 cm3 針筒頂部,用電烙鐵和透明熱縮膠管保護針筒 (圖 94)。近針筒咀部鑽兩小孔方便釋放壓力,利用 “Blu Tack” 泥膠封口 (圖95),其組合作用有如栓塞。
(3) 銅和鎳鉻合金線不能以錫焊接,只可以靠直接接觸。方法是用剛好大小的熱縮膠管重複地箍死,再用填料混合膠封口 (圖 96) 。組合便是一條電解電極。
(4) 製備之電極透過針筒咀,再用填料混合膠封口 (圖 97),完成一單元可收集氣體電極棒。
(圖 90) | (圖 91) | (圖 92) | (圖 93) |
(圖 94) | (圖 95) | (圖 96) | (圖 97) |
(5) 兩組製備之組合放入有兩孔之PVC膠板條,再用填料混合膠粘死。完成之電極可以進行電解 (圖 98) 。
(6) 裝置剛好放於一100 cm3 燒杯 (圖 99) 。
䦕始實驗
(1) 首𠀡置約 80 cm35M NaCl溶液於100 cm3 燒杯,用小量 “Blu Tack” 封死兩針筒管之小孔。雙手拿著組合,引升一點,證實管內溶液沒有下降才為合格,即沒有氣壓差 (圖 100)
(2) 開始電解 (圖 101) 。
Electrolysis
(圖 98) | (圖 99) | (圖 100) | (圖 101) |
各類測試
(a) 氧氣和氫氣之容積比例 (參考實驗 15)

(圖 102) 氧/氫1:2 容積比
1 : 2 Volume ratio of O2 to H2
(b) 測量生成之鹼性氫/氧燃料電池之電動勢 (參考實驗 15)

(圖 103) 鹼性氫/氧燃料電池起始電動勢
Measurement of e.m.f. of the generated alkaline fuel cell
(c) 測量氫氣 (爆鳴) (參考實驗 15)

(圖 104) (爆鳴) 實驗
“Pop” sound test
(d) 測量氧氣 (參考實驗 15)
 (圖 105) 測量氧氣
(圖 105) 測量氧氣
Test for oxygen gas
實驗 (15) 定性和定量小型電解儀器 –「電解管」 (109頁)
4.5 微型測量燃燒熱套件 (microscale heat of combustion kit) 及建議實驗 (16)
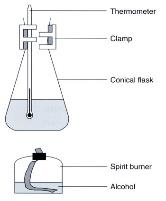
(圖106) 傳統燃燒熱測量裝置
傳統燃燒熱測量裝置
上圖是一般中學測量乙醇燃燒熱或燃燒摩爾焓變之化學實驗裝置。稱量已燃燒了的乙醇 (ethanol量度錐形瓶水溫度上升的幅度便可用公式 ΔH = ms (ΔT) 計算乙醇之燃燒熱。實驗結果和文獻誤差相當大,主要原因是實驗進行時有熱流失。
測定乙醇燃燒熱不一定要用水加熱,加熱固態物件如金屬鋁也可以。微型燃燒熱測量套件用「雙實驗校對」技巧,基本消除實驗時之熱流失 (參考實驗16)
 |  |
| (圖107) | (圖108) |
燃燒摩爾焓變指可燃對象完全燃燒時釋放之熱能。汽油燃燒發熱,提供內燃機動力。碳水化合物燃燒 (即消化 + 吸收 + 血氧作用) 則提供人類器官運動能量。測量可燃物質之燃燒摩爾焓變一般是把它真實地燃燒起來,所產生的熱能令另外一件物件溫度上升,從而計算可燃物質之燃燒摩爾焓變。
微型燃燒熱測量套件由 (i) 玻璃小砵, (ii) 鋁塊熱量計和 (iii) 溫度計組成 (圖107, 108)。
鋁塊熱量計之製作
取一節實心圓鋁條,長 26 mm,直徑 38 mm, (圖109)。一面正中鑽一個直徑6.2 mm洞,深度剛好放入一溫度計 (圖110)。另一面邊緣三對稱處各鑽一個直徑3.8 mm洞容納一節直徑3.8 mm長30 m鋁條 (這鋁條取自一根6.2 x 13 mm拉釘)。這面正中造一個直徑約15 mm坑,目的是增加火熖和鋁塊之接觸面積。
把這三條小鋁條分別放入三個小洞,突出約20 mm,再用環氧樹脂混合膠黏牢,作用像三隻腳 (圖111)。
|
|  |
(圖109) | (圖110) | (圖111) |
實驗 (16):測定propan-1-ol (1-甲基乙醇) 的燃燒摩 爾焓變 (114頁)
4.6 熔度計 (meltometer)
熔度計套件 (圖114, 115) 為一設計新穎之溶點測量儀。與一般用油加熱 (圖 112 ) 或用電加熱 (圖 113 ) 之溶點測量儀不同,它只簡單地用一大一小試管形成之空氣空間直接用本生火熖加熱。熔度計可測量高熔點或低熔點之固體,視乎儀器温度計之測量範圍。熔度計較其他溶點測量儀更快地加熱和冷卻。
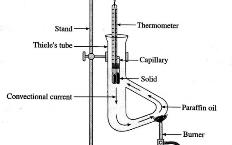 |  | 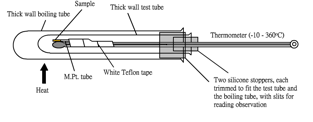 |
| (圖112) | (圖113) | (圖114) 熔度計 |
(圖115) | (圖116) | (圖117) | (圖118) |
| 熔度計套件之組合有: | 1. 一厚身試管 2. 一厚身大試管 3. 一水銀注入式温度計 (-10 – 360o C) 4. 兩個矽膠塞,分別修剪至合適試管和大試管 5. 一卷水喉膠布 6. 一把金屬製放大鏡 7. 一小試管內裝10支熔點管 |
熔度計套件操作非常直接和簡單
1. 戴上安全措施眼鏡
2. 把粉狀固體樣本放入熔點管
3. 剪一段水喉膠布把熔點管貼近温度計之球部位置 (圖118)
4. 利用小矽膠塞置熔點管/温度計組合於試管中
5. 利用大矽膠塞再置試管/熔點管/温度計組合於大試管中,容許兩試管一些空間
6. 調校大小矽膠塞之位置令觀察温度不受障礙 (圖117)
7. 稍稍傾斜整個組合並用鐵架夾緊 (圖116)
8. 用大本生火熖加熱整個組合之底部
9. 用附有之放大鏡觀察樣本之狀態
10. 當接近熔點時停止加熱
11. 當樣本變為熔液時 (呈透明狀) 記錄温度讀數
12. 拆除裝置 (還在高溫狀態),冷卻回室溫
13. 重覆實驗,取得可靠結果
注意:實驗完畢後應等待足夠時間令裝置完全冷卻才可放回容器裏